
Privacy statement: Your privacy is very important to Us. Our company promises not to disclose your personal information to any external company with out your explicit permission.
Компания Suyzeko исследовала новый продукт. Brain Photobiomodulation Machine, наша компания потратила более 1 года, чтобы исследовать продукт, и мы пригласили профессора провести исследование для нас. Смотрите следующую статью для деталей.
Исследовательский отдел для дополнительной и интегративной лазерной медицины, исследовательского отделения биомедицинской инженерии в области анестезии и медицины интенсивной терапии, а также исследовательский центр TCM Грац, Медицинский университет Грац, Auenbruggerplatz 39, EG19, 8036, Австрия
Получено: 4 января 2019 г. / принято: 15 января 2019 г. / Опубликовано: 16 января 2019 г.
фотобиомодуляция; мозг; Стимуляция светодиодного (светооборота); легкая терапия; Длина волны; Инсульт; деменция; психические заболевания; Региональное насыщение головного кислорода; тепловая визуализация; Светодиодный шлем
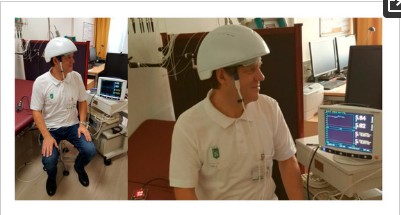
Рисунок 1. Первое измерение с инновационным светодиодным (светооборотным диодом) шлема фотобиомодуляции (прототип от Suyzeko (Shenzhen Guangyang Zhongkang Technology Limited, Китай)) в исследовательском центре TCM в Медицинском университете Грац, Австрия, Европа, исполненная 25 декабря 2018 года. Анкет
Оборудование в настоящее время основано на инфракрасном светодиоде с использованием длины волны 810 нм. Эта длина волны была доказана в последнее время (2018) как одна из лучших для транскраниальной лазерной/световой стимуляции [9]. Результаты были подтверждены измерениями, выполненными нашей исследовательской группой [5,6,7,8,10].

Измерения изменений в региональном насыщении головного кислорода (RSO2) проводились с использованием инструмента ONVOS 5100C Oximeter (Somanetics Corp., Troy, MI, USA). Приблизительная инфракрасная спектроскопия является неинвазивным методом измерения RSO2HOUGHTH Интактный череп, который успешно применялся в основных медицинских исследованиях и клинических показаниях в течение многих лет [6]. Светлый свет (730 и 805 нм) испускается через кожу, и после прохождения различных видов ткани (кожа и кости) возвращаемый свет обнаруживается на двух расстояниях от источника света (3 и 4 см). Основываясь на этом принципе, спектральное поглощение крови в более глубоких структурах (2–4 см) может быть определено и определено как RSO2 [5,12]. Датчики были нанесены в лобную зону на правой и левой сторонах мозга здорового добровольца (см. Рисунок 1). Чтобы свести к минимуму влияние внешнего света, голова в этой области была покрыта эластичной полосой во время процедуры записи и стимуляции. После 20 -минутного времени отдохнула светодиодная стимуляция включена. Результаты трех секций (до (20 мин), в течение (15 мин) и после (20 мин)) показаны на рисунке 3. Обратите внимание на значительное увеличение RSO2 (слева и правая) во время и даже после транскраниального Светодиодная стимуляция. Изменения температуры показаны на рисунке 4.
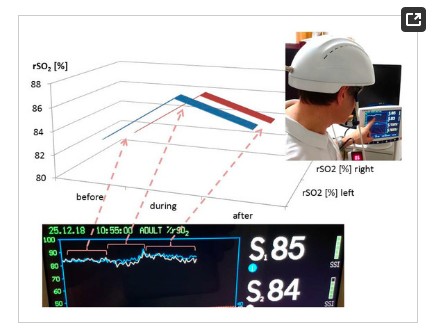
Рисунок 3. Результаты первого пилотного измерения с помощью светодиодного стимуляционного шлема от Суйзеко (Шэньчжэнь, Китай). Обратите внимание на увеличение регионального насыщения головного кислорода во время и после стимуляции на левой и правой стороне.

Терапия PBM была разработана более 50 лет назад; Тем не менее, до сих пор нет общего согласия по параметрам и протоколам для его клинического применения. Некоторые исследовательские группы рекомендовали использовать плотность мощности менее 100 мВт/см2 и плотность энергии от 4 до 10 J/см2 [11]. Другие группы рекомендуют до 50 J/см2 на поверхности ткани [11]. Такие параметры, как длина волны, энергия, флюенс, мощность, излучение, режим импульса, продолжительность лечения и скорость повторения, могут применяться в широком диапазоне. Наши нынешние предварительные результаты показали четкую реакцию церебрального RSO2 в отношении стимуляции светодиодов. Тем не менее, необходимо упомянуть, что температура значительно увеличилась, и эти эффекты должны учитываться в дальнейших исследованиях. Существует также тот факт, что неэффективные исследования в клетках с высокой митохондриальной активностью, по-видимому, чаще связаны с переосмыслением, чем с недостаточной дозировкой [11]. Поэтому необходимы клинические исследования, касающиеся оптимальных доз стимуляции.
Транкраниальный PBM кажется многообещающим для лечения различных психических заболеваний. Pitzschke et al. [13] также измерили распространение света в различных областях заболевания Паркинсона (PD), относящейся к глубокой мозговой ткани во время транскраниального и трансфеноидального освещения (при 671 и 808 нм) головки трупа и смоделированные оптические параметры ткани человека с использованием Монте- Симуляции Карло. Это исследование демонстрирует, что можно также осветить глубокие ткани мозга транскраниально и трансфеноидально. Это открывает терапевтические варианты для страдающих БП или других заболеваний головного мозга, требующих легкой терапии [13].
Было проведено несколько исследований, касающихся возможных побочных эффектов для светодиодного PBM. Например, Moro et al. Исследовали эффекты долгосрочного применения до 12 недель PBM (670 нм) в нормальных наивных макак -обезьянах. Они не нашли гистологической основы для каких -либо серьезных проблем с биобезопасностью, связанными с PBM, предоставленным внутричерепным подходом [14]. Хеннесси и Хамблин также указали на уже установленную безопасность и заметное отсутствие побочных эффектов транскраниальной ПБМ [2].
Предварительные результаты очень многообещающие; Однако необходима дальнейшая исследовательская работа, чтобы иметь возможность использовать, например, этот новый вид PBM в качестве терапевтического метода. Многие исследователи считают, что PBM со светодиодным и/или лазером для расстройств мозга станет одним из наиболее важных медицинских применений легкой терапии в ближайшие годы и десятилетия [3].
Автор не объявляет конфликт интересов.
LET'S GET IN TOUCH

Privacy statement: Your privacy is very important to Us. Our company promises not to disclose your personal information to any external company with out your explicit permission.

Fill in more information so that we can get in touch with you faster
Privacy statement: Your privacy is very important to Us. Our company promises not to disclose your personal information to any external company with out your explicit permission.